血管网络是机体运输营养物质、氧气及代谢产物的主要系统。因此,血管生成对于生命系统的正常运转具有重要意义。血管生成的核心过程是血管内皮细胞的出芽生长和管腔形成,由内皮细胞膜表面生长因子受体感知微环境的生理及病理变化后通过生长因子信号网络调控。然而,这些信号的协同调控机制尚不清楚。

2022年6月21日,浙江大学生命科学学院遗传与再生生物学研究所余路阳-裘聪课题组在PNAS在线发表了题为“FGFR1 SUMOylation coordinates endothelial angiogenic signaling in angiogenesis”的研究论文。该研究揭示了内皮FGFR1的动态SUMO化修饰通过调控血管生成核心通路VEGF/VEGFR和FGF/FGFR的平衡,进而使机体完成不同微环境下的血管生成。
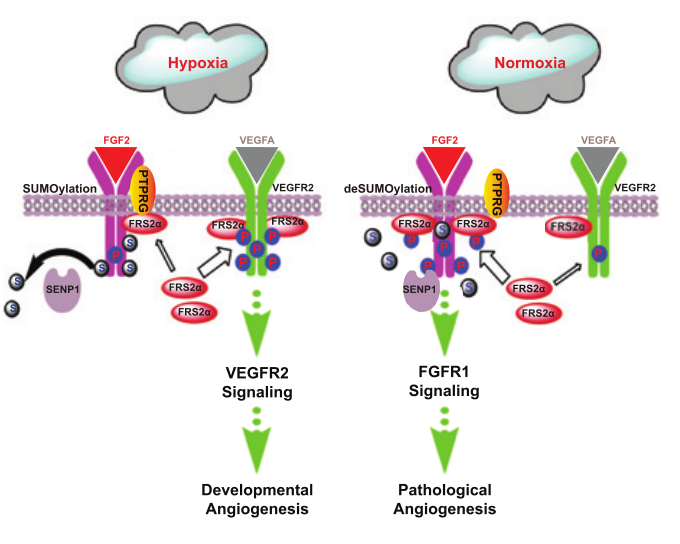
在这项工作中,作者们发现了血管内皮细胞中成纤维细胞生长因子受体1(FGFR1,其配体FGF2为首个被发现的促血管生成因子)保守的赖氨酸位点发生响应于血管生成刺激的蛋白翻译后SUMO化修饰;该过程由去SUMO化酶SENP1调控。缺氧环境能增强FGFR1的SUMO化,进而通过限制 FGFR1 的二聚化和FGFR1与其磷酸酶 PTPRG 结合来抑制FGFR1酪氨酸激酶的活化。由此,保证了酪氨酸激酶受体的锚定蛋白FRS2α被血管内皮生长因子受体2 (VEGFR2)招募,而限制了FGFR1对FRS2α的招募,支持了内皮细胞中 VEGFA/VEGFR2 信号的激活。另一方面,常氧下病理组织中FGF2的累积会引发FGFR1的去SUMO化并促进FGFR1招募额外的FRS2α 募集,从而高度激活 FGFR1 信号以支持常氧环境下的血管生成。因此,SENP1调控的FGFR1 SUMO化/去SUMO化作为内在机制调控了FGFR和VEGFR受体复合体激活转换和下游血管生成信号的平衡。FGFR1的SUMO化缺陷突变体在人原代内皮细胞和小鼠中对血管生成功能的抑制性效应进一步证实了上述结论。
结合课题组之前发表的NOTCH的SUMO化调控是血管生成重要负向调控机制(Circulation Research 2017),这些发现揭示了血管生成信号网络未知的协同机制,阐明了SUMO化修饰在血管发育和修复中的重要作用。余路阳教授为该论文的通讯作者,课题组已出站博士后朱晓龙博士(目前在耶鲁大学担任Associate Research Scientist)和裘聪副研究员为本文共同第一作者,2017级博士生王怡然为主要作者,科研团队的多位学生在文章返修过程中都有积极贡献。该项目得到国家自然科学基金委、国家重点研发计划、浙江省自然科学基金委、浙江大学“世界顶尖大学合作计划”等的资助。