研究背景
脊髓损伤是一类严重的中枢神经损伤,导致损伤平面以下感觉和运动功能部分或完全丧失[1]。脊髓损伤不仅造成严重的组织损伤,还严重扰乱了脊髓神经回路的兴奋性/抑制性平衡,对脊髓的正常功能产生极大影响[2,3]。尽管人类脊髓损伤幸存者极少出现完全脊髓损伤,但许多情况下患者仍表现出偏瘫等严重后遗症。因此,如何激活损伤后残留的神经回路发挥功能,一直是该领域的研究重点。研究显示,通过药物或物理手段恢复脊髓神经回路的兴奋性/抑制性平衡,可以有效修复脊髓功能[2,4,5]。比如,近年来,瑞士联邦理工学院Grégoire Courtine教授团队开发的脑-脊髓接口装置通过灵活调控残留神经回路,使瘫痪患者实现自然站立和步行[5],这一重大突破显示了调控残留神经环路的巨大潜力。
然而,这类装置的临床转化仍面临三大难题:1)价格昂贵,难以实现大规模应用;2)不能应用于急性期的脊髓损伤的治疗;3)无法在损伤的急性期提供神经保护作用,让更多的神经环路存活下来。相比之下,药物治疗方式更具广泛临床应用的潜力,如针对KCC2靶标的激动剂CLP257已显示出促进脊髓损伤后功能恢复的作用[2]。但是,该治疗方法还存在无法靶向特定的神经环路,生物利用度低,不能提供神经保护作用等问题。因此,开发高效、有神经环路靶向性和神经保护作用的药物,用于急性期的脊髓损伤治疗,对脊髓损伤患者的预后及功能恢复至关重要。
摘要
2023年06月12日,浙江大学脑科学与脑医学学院王绪化研究员课题组在Nat. Nanotechnol.上发表了题为“Controlled delivery of a neurotransmitter-agonist conjugate for functional recovery after severe spinal cord injury”的研究。该团队开发了一种静脉注射纳米药物,通过靶向抑制性神经元调控其过度兴奋状态,平衡了紊乱的残余脊髓环路,并通过调节损伤环境,提供了神经保护作用,最终成功促进脊髓损伤后运动功能的恢复。该研究为中枢神经系统损伤后的药物调控提供理论依据,为广泛高效的脊髓损伤治疗提供了新思路。
纳米药物能极大提高药物溶解性,延长体内循环时间等性能,因此团队提出构建一种纳米调控药物。针对损伤环境的高浓度活性氧(reactive oxygen species,ROS),设计ROS响应性的纳米药物。此外,通过巧妙的神经递质修饰,为纳米药物增添靶向神经元亚型的功能。研究团队测试了两种不同神经元,多巴能神经元(DOPA)、γ-氨基丁酸(GABA)能神经元,靶向纳米药物的最终效果。实验结果发现针对GABA能神经元的纳米药物能够有效调控神经元兴奋状态,保护残留神经组织,促进脊髓损伤后的功能恢复。
或许,脊髓损伤病人在不久未来能够用上价格适宜、普适性更强,且具备神经保护作用的高效药物。这项研究成果让脊髓损伤患者看到了更可及的治疗手段,而不必依赖昂贵的神经接口技术,这为脊髓损伤患者康复带来了新希望。

研究结果
如图1和2所示,研究开发的智能纳米药物具备良好的纳米尺寸(~100nm),高效的ROS响应能力。在体内环境能有效向脊髓损伤部位聚集,且靶向性能良好(~80%)。此外,纳米药物至少能够在注射24小时内维持较高浓度,这使其有望在脊髓损伤后急性期发挥疗效。
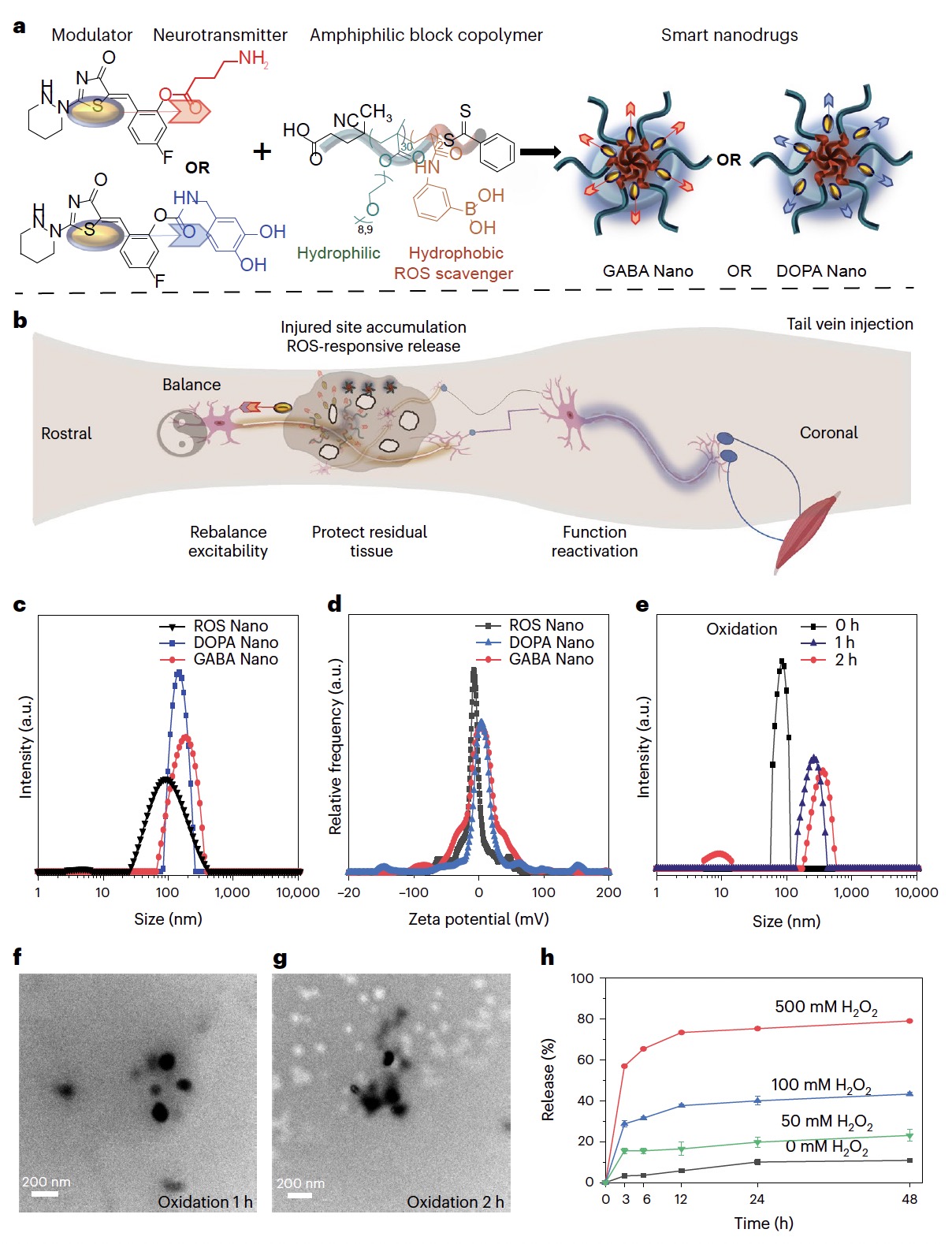
图 1.智能纳米药物的合成和表征。
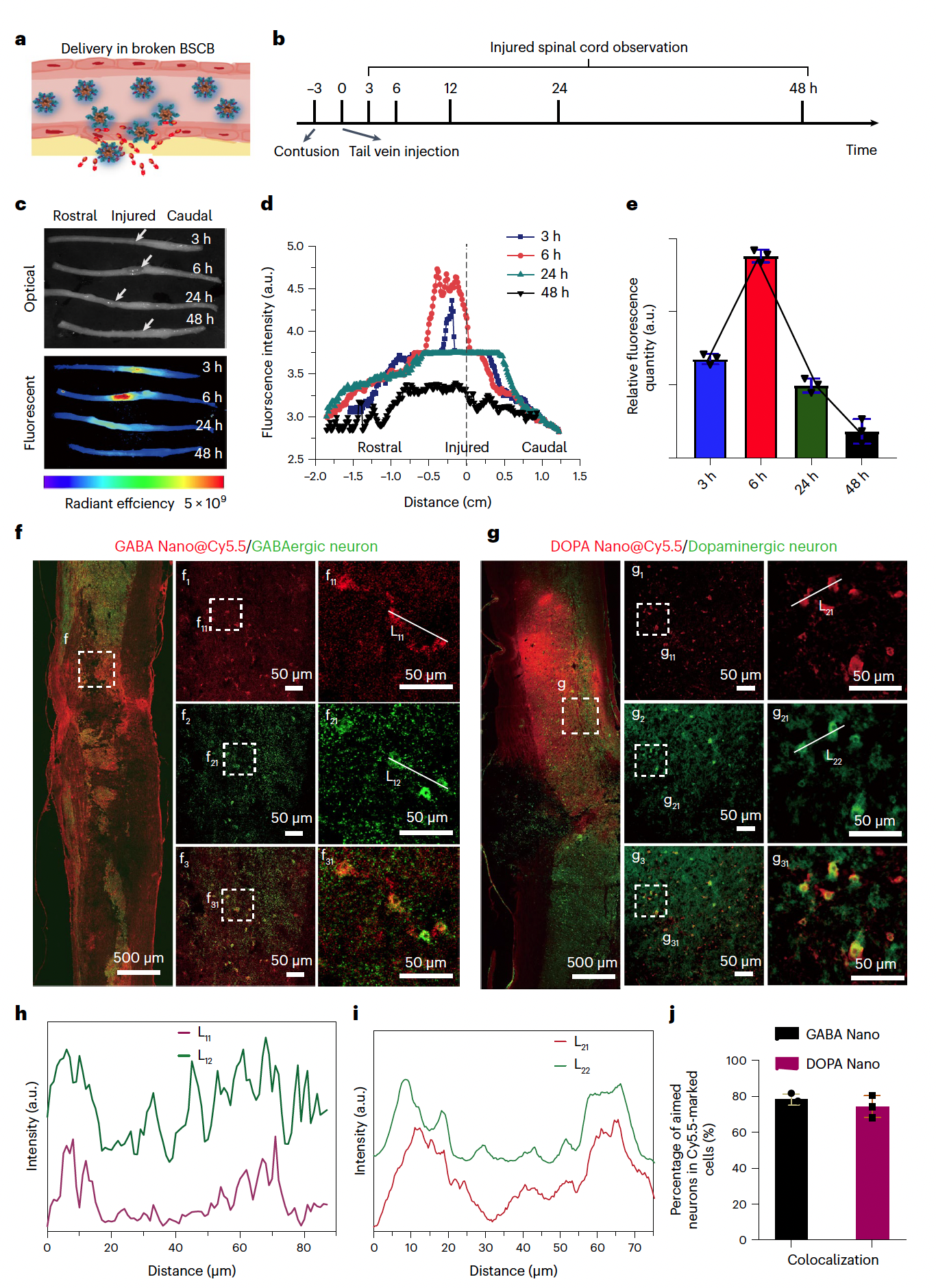
图 2.智能纳米药物在脊髓损伤部位聚集,并选择性地靶向特定神经元及神经环路。
在验证了纳米药物的递送功能后,研究对设计的双功能纳米药物的实际疗效进行了更系统的评价。如图3所示,在治疗组中,仅GABA Nano组大鼠在损伤后能够实现更明显的功能恢复。尽管ROS Nano和DOPA Nano组的大鼠运功相对于对照组有一定的恢复,但GABA Nano组大鼠的后肢运动的各项指标都优于其他组大鼠,也更接近正常大鼠。这些结果表明,在研究设计的纳米药物中,GABA Nano能够实现神经调控并发挥神经保护效果,帮助脊髓损伤大鼠获得最终的运动功能恢复。
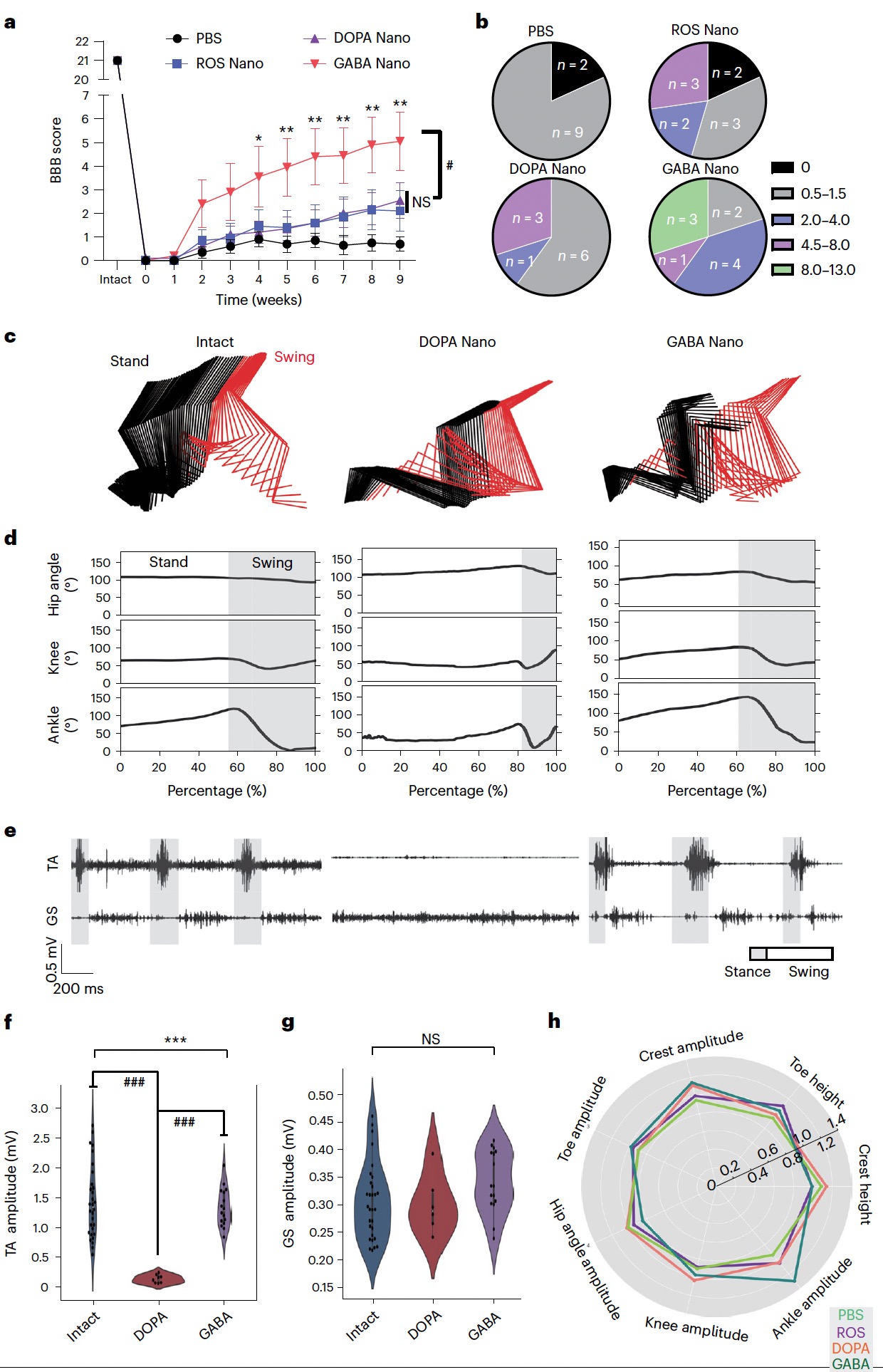
图3. GABA-Nano纳米药物治疗可改善严重挫伤性脊髓损伤大鼠后肢运动功能的恢复。
综上,如图4所示,该研究不仅开发了一种智能的神经调控纳米药物,并通过其神经保护和神经调控的双功能,促进了脊髓损伤后的功能恢复。这为脊髓损伤后的药物治疗研究指出了新模式,为提高脊髓损伤患者运动功能的恢复提供了新的有效方法。研究结果表明,开发价格适宜、普适性更强的高效脊髓损伤治疗药物的正确思路之一,就是通过提高神经调控靶向性并辅以神经保护功能,促进脊髓功能的恢复。该研究成功构建了一种双功能纳米药物GABA Nano,能够在脊髓损伤后有效靶向GABA能神经元,调控其兴奋性,同时提供神经保护作用,从而实现功能修复。
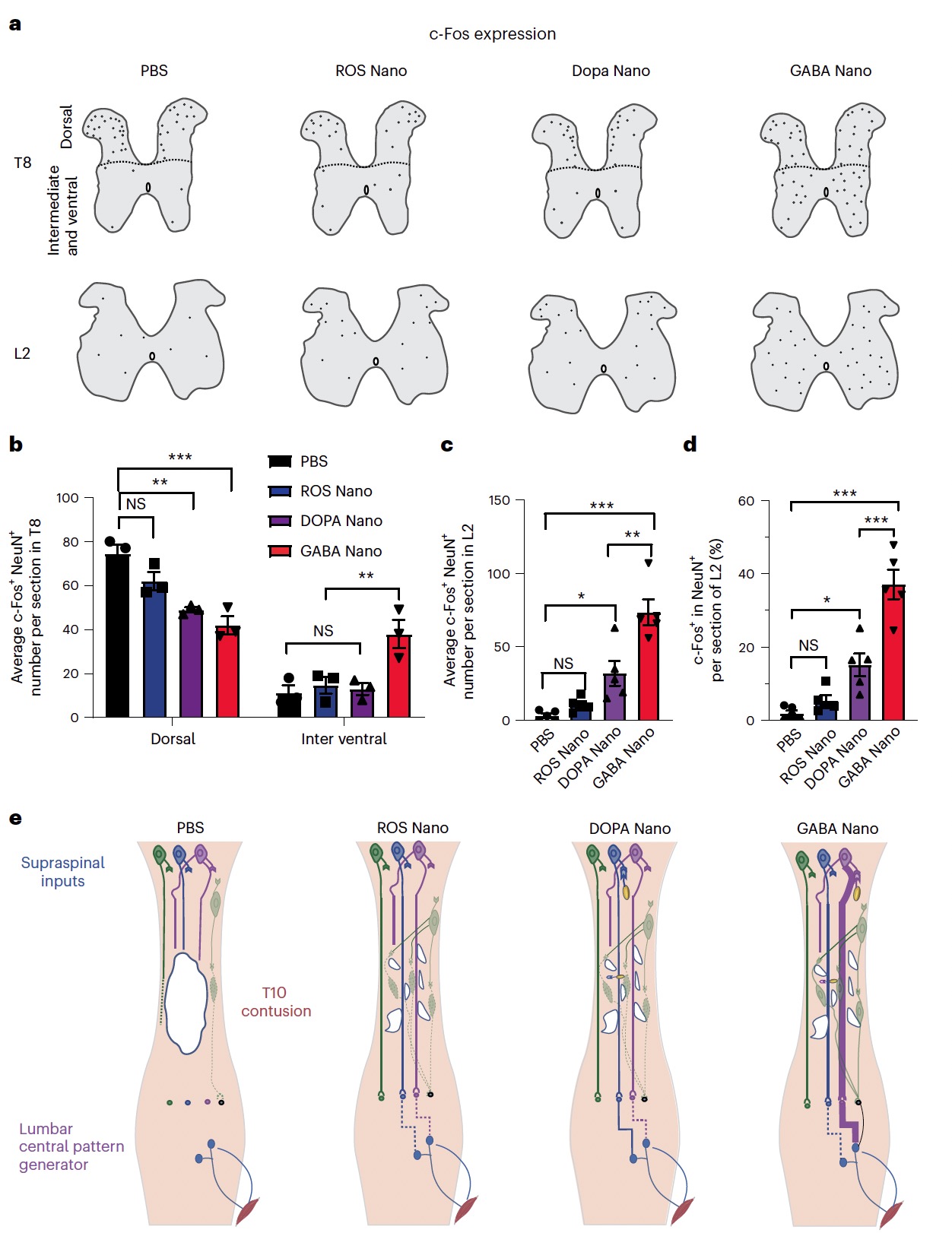
图4. GABA-Nano纳米药物治疗改善严重挫伤性脊髓损伤大鼠后肢运动功能的恢复的机制。
研究展望
尽管目前研究团队研发药物已经有了一定的治疗效果,但针对脊髓损伤药物的开发还有很大提升空间。后续的研究过程中,王教授团队已经通过团队独立研发的人工智能小分子设计平台FeatNN,从由数百万种化合物组成的化合物库中筛选出了更高效的KCC2激动剂,其调控效果相较于CLP-257至少提高了数倍。这有望进一步提高GABA Nano的治疗效果,实现更完全的功能修复作用。
总之,人工智能技术和多靶点精准调控策略将成为王教授团队后续研究的两大利器。未来,他们将继续优化GABA Nano及开发其他新型神经调控纳米药物,力争在3-5年内成功将一款安全高效的脊髓损伤治疗药物推向临床转化,造福更多脊髓损伤患者。
原文链接:https://www.nature.com/articles/s41565-023-01416-0
通讯作者简介
王绪化,浙江大学医学院脑科学与脑医学学院研究员。实验室主要研究治疗中枢神经系统疾病的药物及药物递送系统。主要研究兴趣包括:大语言模型、基于人工智能技术的药物设计和AAV基因递送载体的设计开发,脑机接口及组织工程技术。实验室详情请参考实验室主页(www.zjuwanglab.com)。
该研究得到南通大学顾晓松院士及其团队的大力支持。感谢浙江大学段树民院士在论文修改过程中提出的宝贵意见,并为项目开展提供有力支撑。该研究获得国家科技创新2030-“脑科学与类脑研究”重大项目、国家自然科学基金、浙江省杰出青年科学基金、中央高校基本科研业务费专项等基金的资助。
参考文献
1.Ahuja, C.S. et al. Traumatic spinal cord injury. Nat Rev Dis Primers 3, 17018 (2017).
2.Chen, B. et al. Reactivation of Dormant Relay Pathways in Injured Spinal Cord by KCC2 Manipulations. Cell 174, 521-535 e513 (2018).
3.Anderson, M.A. et al. Natural and targeted circuit reorganization after spinal cord injury. Nat Neurosci 25, 1584-1596 (2022).
4.Rowald, A. et al. Activity-dependent spinal cord neuromodulation rapidly restores trunk and leg motor functions after complete paralysis. Nat Med 28, 260-271 (2022).
5.Lorach, H. et al. Walking naturally after spinal cord injury using a brain-spine interface. Nature (2023).